 |
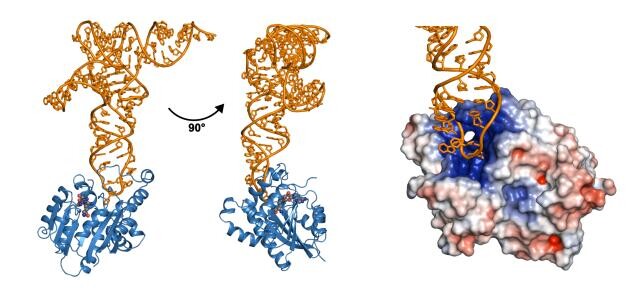
| ▲ 연구팀이 밝혀낸 효소 CmoM과 기질 tRNA 복합체 구조 (사진=광주과학기술원 제공) |
[mdtoday=남연희 기자] 국내 연구진이 생명현상 핵심인 단백질 합성과정에 관여하는 ‘운반 RNA(tRNA)’의 화학적 변형 기작 및 필수 요인을 규명했다.
운반 RNA는 유전자 발현을 통한 단백질의 합성에 관여하는 RNA로 유전자 암호를 해독하고 아미노산을 전달하는 역할을 한다. 또한 현재까지 결정화에 사용된 기질인 세린-특이적 tRNA의 온전한 고해상도 구조도 알려진 바가 없었는데 이번 연구의 공결정(co-cocrystal) 구조 규명으로 세계 최초로 확인됐다.
광주과학기술원(GIST) 화학과 김정욱 교수 연구팀은 tRNA 안티코돈 워블 유리딘에서 CmoM 효소에 의한 화학적 변형 기작과 필수 요인들을 규명했다고 27일 밝혔다.
연구팀은 효소-tRNA 복합체 구조를 바탕으로 생체 내 화학적 변형에 대한 연구를 수행했다.
단백질은 우리의 몸을 구성하는 핵심 요소이다. 단백질을 만드는 유전정보가 들어있는 DNA가 RNA 형태로 복사된 뒤 단백질 생산 공장인 리보솜으로 전달돼 다양한 형태와 기능의 단백질이 만들어진다. RNA는 이 과정에서 핵심 역할을 담당한다.
세포 내 정상적으로 작동하는 단백질을 합성하려면 리보솜(ribosome)에서 tRNA에 의한 번역과정이 오류 없이 일어나야 하는데, 그렇지 못한 경우 잘못된 단백질이 합성되어 생명 유지에 필수적인 작용들이 일어날 수 없게 된다.
tRNA가 효과적으로 기능하기 위해서는 tRNA 분자 내에 화학적 변형이 선행되어야 한다. 각각의 화학적 변형은 서로 다른 tRNA 변형 효소에 의해 조절된다.
tRNA 변형이 진행되지 않으면 제대로 된 단백질 합성이 어려워지고 궁극적으로 생명 유지에 치명적일 수 있어 tRNA 변형의 역할 및 효소의 조절 기작을 이해하는 것은 매우 중요하다. tRNA 변형의 원리는 기질 tRNA와 결합된 변형 효소가 이루는 복합체의 구조를 얻음으로써 가장 효과적으로 이해할 수 있다.
생화학 분야에서 구조 연구에 이용되는 X-선 결정학은 반세기 넘게 마이오글로빈을 시작으로 수많은 단백질과 핵산 등의 구조를 밝혀냈지만 안정적인 단결정이 있어야 분석이 가능하다.
특히 단백질과 RNA의 복합체는 결정화하기 쉽지 않은데, 생체 분자의 구조들이 등록되어있는 데이터베이스(Protein databank, PDB)에 따르면 단백질-RNA 복합체의 구조가 차지하는 비율은 전체 5% 정도에 불과하다.
연구팀은 CmoM 효소와 세린-특이적 tRNA의 고해상도 공결정 구조를 X-선 결정학을 통해 규명하고, 이 구조를 통해 효소가 어떻게 기질인 tRNA를 선택적으로 인식하고 메틸기를 안티코돈 워블 유리딘에 전달하는지 확인했다.
세린-특이적 tRNA가 지니고 있는 안티코돈 워블 유리딘 위치는 화학적 변형이 다른 위치에 비해 극심하게 일어나고 유전자 암호 해독에 특히 중요하다고 알려져 있다.
지금까지 복합체 구조가 부재해 CmoM 효소의 작동원리 및 메틸기를 받아들이는 기질 tRNA를 원자 수준에서 이해하기에 많은 한계가 있었는데, 연구팀이 새로운 구조를 밝혀냄으로써 이 한계를 극복한 것이다.
연구팀은 대장균(E. coli)에서 과발현된 CmoM 효소와 세린-특이적 tRNA를 정제했고, 메틸전달 대사물질인 SAM의 유사체인 sinefungin을 사용해 공결정을 제작, X-선 결정학 실험을 통해 그 구조를 규명했다. 이 구조에 의하면 CmoM은 tRNA 분자의 전체적인 형태보다는 안티코돈이 위치한 루프와만 주로 상호작용하며 특이적으로 결합하는 것으로 밝혀졌다.
또한 효소에 기질 tRNA가 결합하면서 CmoM의 일부 구조의 재배치가 일어나 tRNA를 감싸는 형태 변화가 일어났으며 tRNA도 마찬가지로 안티코돈 루프의 형태가 복합체를 이루며 국지적으로 변한 것을 확인할 수 있었는데 특히 워블 유리딘이 효소를 향해 상당히 젖혀진 형태로 활성 부위에 결합되어 있었다.
공결정 구조를 통해 파악한 tRNA와 상호작용하는 CmoM 효소의 아미노산 잔기들을 점돌연변이 시켰을 때 효소의 tRNA 변형 능력이 크게 감소하거나 아예 사라짐을 관측하여 X-선 구조에서 얻은 정보를 기능적으로 확인할 수 있었다.
김정욱 교수는 “이번 연구 성과는 단백질 번역에 필수적인 tRNA, 그리고 tRNA 변형에 관여하는 단백질 효소의 구조 기반 메커니즘 연구로 생체 내에서 변형 활성이 어떻게 일어나는지, 또한 변형이 부재하면 어떤 결과가 초래되는지를 이해하는 데 중요한 실마리를 제공할 것”이라고 말했다.
이번 연구는 한국연구재단(NRF) 개인연구지원사업(중견)의 지원을 받았으며, 생화학 분야 국제학술지인 ‘Nucleic Acids Research’에 2023년 8월 17일에 온라인 게재됐다.
메디컬투데이 남연희 ([email protected])

[저작권자ⓒ 메디컬투데이. 무단전재-재배포 금지]
















































