 |
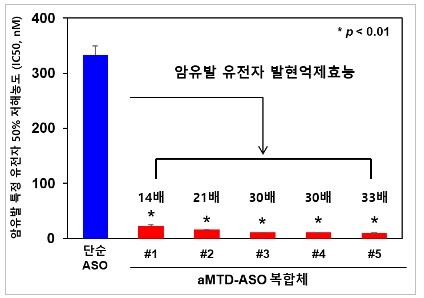
| ▲TSDT 플랫폼기술이 적용된 펩타이드-핵산 복합체 (aMTD-ASO conjugate)가 세포 내부로 전송되어 암유발 특정유전자 발현억제효능이 증명 (사진=셀리버리 제공) |
셀리버리가 아시아 혁신제약사 1위인 글로벌 제약사의 요청으로 현재 공동개발중인 유전자간섭 안티센스 올리고핵산(antisense oligonucleotide: ASO) 항암신약의 세포내 전송 및 대장암/폐암/유방암 유발 특정유전자의 발현억제효능 검증 최종결과보고서 및 2차례 추가검증보고서가 각각 이 글로벌 제약사에 통보된 후, 이 제약사로부터 재현성만 입증되면 성공으로 판정할 수 있으며, 그 다음 단계 진입 가능성이 매우 높다는 통보를 받았다고 3일 밝혔다.
셀리버리는 매출액 기준 아시아 2위 글로벌 제약사에게 aMTD-ASO 접합체 (conjugate)가 인간 폐암세포에서 대장암/폐암/유방암 유발 유전자의 발현저해능이 단순 ASO 대비 3배에서 최대 15배까지 유전자 넉다운 (knockdown: KD) 효능을 갖는 연구결과를 통보했고, 상대측의 판단을 기다린다는 언론보도가 있었다.
그러나, 이 글로벌 제약사 측은 aMTD-ASO의 효능에는 만족함을 보였지만 단순 ASO와 aMTD-ASO 접합체의 특정유전자 발현억제능의 직접 비교실험 (target gene KD activity comparison study)과 농도 의존도실험 (dese dependency study) 등 추가 검증시험들을 다시 요구했다고 밝혔다.
셀리버리의 조대웅 대표는 “보수적인 아시아 제약사 특성상 연구결과에 대해 매우 조심스러워 하며 결과에 대한 계속적인 검증을 요구할 것으로는 예상 했지만, 이번 공동개발은 생각보다도 더 많은 추가에 또 추가 데이터 검증요구로 지연이 발생되고 있는 상황이다. 따라서, 회사차원에서 신속히 다음단계 진행을 하지 않을 경우, 우리 쪽에서 프로젝트를 중단하겠다라고 강하게 대응했다” 라고 배경을 설명했다.
이어 조 대표는 “셀리버리의 제3세대 세포막 투과 펩타이드 aMTD가 ASO 올리고핵산에 화학적으로 결합된 aMTD-ASO 접합체는 빠른 시간 내에 세포막 직접투과 메카니즘으로 세포내 전송이 가능하기 때문에, aMTD가 접합되지 않은 단순 ASO가 세포식포작용으로 전송되지 못하는 조건 (1시간 투여) 에서 aMTD-ASO의 유전자 발현저해 넉다운 활성이 단순 ASO에 비해 최대 37배까지 향상시킴을 증명했다” 라고 밝혔다.
“반대로 오랜시간 (48시간 이상) 투여하는 조건에서도 세포식포작용을 못하게 하는 식포작용저해제 (endocytosis inhibitor)를 동시 처리하여 단순 ASO에 비해 aMTD-ASO가 최대 33배까지 암발병 유전자 넉다운 효능을 나타낸 것을 농도의존적으로 추가 증명하여, 이 제약사가 원했던 모든 조건에서의 ASO와 aMTD-ASO 와의 직접 비교시험 결과를 추가로 통보했다” 라고 덧붙였다.
“또한, aMTD-ASO 접합체만이 세포간 연속전송이 가능함을 증명한 데이터를 이 글로벌 제약사 측에 또 다시 추가로 통보 함으로써, 당사는 이제 최종보고서에 이어 추가 및 재추가 보고서까지 할 수 있는 모든 데이터를 완벽히 제시하였으므로 사업의 중단이던, 또는 앞으로의 사업의 성공 (최종 라이센싱 아웃: L/O) 이던, 어떤 결과가 나오더라도 우리기술 및 우리연구진의 노고에 만족하고 있고 상대측의 재현 검증결과를 기다리고 있다” 라고 설명했다.
이러한 일련의 추가검증결과 보고서를 검토한 이 제약사의 공동개발 책임자는 “이번 결과는 다음단계로 진입하는데 충분하다고 사려된다” 라고 반응했으며, “마지막으로 자사 연구소에서 재현성을 확인하고 싶다, 자세한 실험 프로토콜을 제공해 달라” 라고 요청해 왔다고 밝혔고, 현재는 제공된 셀리버리의 실험프로토콜을 토대로 이 제약사 신약연구소에서 재현성 검증시험중인 것으로 알려졌다.
재현성이 증명된다면, 이번 공동개발 평가시험은 성공으로 판단될 것이고, 다음단계가 진행될 것으로 예상된다.
셀리버리의 공동개발 책임자 신슬미 박사는 “지난 최종보고서 제공 이후에 추가검증시험 요청이 계속 있었고, 이에 대해 상대편이 집요하게 원하던 모든 조건의 추가검증 데이터를 제공한 상태인 만큼, 이 글로벌 제약사도 우리 aMTD 기술에 대한 의심이 이제는 확신으로 바뀐 것을 체감한다” 라고 밝혔다.
“오래되고 전통을 중시하는 아시아 제약사의 보수적인 분위기에 따라 상대측 신약연구소에서 우리 데이터가 재현되는지를 확인하고 있으며, 당사에서 수십 수백 차례 검증 또 재검증 한 결과이므로 크게 다르지 않은 결과가 도출될 것으로 기대하며 판단을 기다리고 있다” 라고 말했다.
메디컬투데이 남연희 ([email protected])

[저작권자ⓒ 메디컬투데이. 무단전재-재배포 금지]
















































