1시간 이내 뇌조직에 신속 전송…"뇌질환치료제 개발 난제 극복"
셀리버리가 파킨슨병 치료제 ‘iCP-Parkin’이 뇌를 지키는 보호막 혈뇌장벽을 통과해 1시간 이내로 신속하게 뇌조직에 전송된다는 것을 증명했다.
셀리버리는 글로벌 위탁연구기관 코방스 (Covance, 영국)의 액체크로마토그래피-직렬질량분석법 (LC-MS/MS)을 이용해 이 같이 입증했다고 4일 밝혔다.
최저정량한계(LLOQ)를 5000만분의 1그람 (20ng/ml) 단위까지 분석하는 정밀분석을 통해 증명한 것으로, 셀리버리는 이로써 TSDT 플랫폼기술로 향상된 약리물질의 뇌 약리동태 (Brain PK)에 대한 객관적인 데이터를 원하던 글로벌 제약사의 요구를 충족시킬 수 있게 됐다.
파킨슨병은 신경전달물질인 도파민을 생성하고 분비하는 뇌신경세포 (neuron)가 손상돼 운동능력과 인지기능에 장애가 생기는 퇴행성 뇌질환이며, 이러한 신경세포 파괴는 알파-시뉴클레인 (α-Synuclein) 단백질의 응집체 (protein aggregate)에 의해 발생한다고 알려져 있다.
파킨슨병의 치료를 위해서는 증상 완화 또는 질병의 진행을 늦추는 약물인 도파민 전구체 레보도파(Levodopa)를 투여해 뇌에서 도파민의 농도를 높여 주는 것이 유일한 약물치료법이나 장기복용 시 부장용과 약물 저항성이 나오는 등 근본적인 치료방법이라 볼 수는 없었다.
때문에 이러한 난치성 뇌질환에 대한 치료제 개발에 어려움을 극복하려 여러 글로벌 제약회사에서는 알파-시뉴클레인을 제거할 수 있는 중화 항체치료제 개발을 시도했으나 실패했다.
이는 뇌를 둘러싸고 있는 혈뇌장벽 (BBB)을 뚫고 뇌조직 안으로 약물을 전송하기가 어려움은 물론, 조금 투과하더라도 뇌신경세포 (neuron) 내부로 항체같이 커다란 약리물질들의 세포 내 투과가 불가능하기 때문이다.
그러나 셀리버리의 ‘iCP-Parkin’은 이러한 거대분자 약리물질들을 생체 내 조직, 그 조직을 구성하는 세포 안으로 약물을 전송시킬 수 있는 플랫폼기술 TSDT를 이용해 혈뇌장벽을 구성하는 혈관 내피세포 (endothelial cell) 세포막 투과에 성공했다.
이어 계속해서 뇌조직을 구성하는 뇌신경세포를 연속 투과해 알파-시뉴클레인 단백질의 응집체의 축적 (Lewy body)을 막아 파킨슨병 치료효능이 뛰어남을 상위 1% 과학저널인 사이언스 어드벤시스 (Science Advances)에 발표해 학계의 검증을 통해 증명한 바 있다.
셀리버리관계자는 “이번 결과에서 보여주는 신속한 혈뇌장벽 투과력과 뇌신경세포 안으로의 전송능력 증명은 도파민을 생성하는 신경세포에 축적되는 알파-시뉴클레인의 제거가 가능하다는 것을 시사하고 있다”고 밝혔다.
셀리버리의 퇴행성뇌질환치료제 개발실 연구책임자는 “이번 분석의 핵심은, “iCP-Parkin이 혈뇌장벽을 얼마나 신속하게 통과해 뇌조직의 심부에 들어가는지를 보여줌에 의의가 있다” 고 강조했다.
또한 “파킨슨병 모델동물에서 8 단계의 시간대별로 iCP-Parkin을 1회 꼬리정맥 주사투여한 뒤 뇌 120개와 혈액 80개의 샘플을 확보하여, 영국의 코방스로 보내 TSDT 기술이 적용된 iCP-Parkin 재조합단백질 뒤쪽 부분 (33개의 아미노산)을 감지해 조직과 혈액에서 iCP-Parkin을 정량적으로 분석했다”고 덧붙였다.
아울러 “파킨슨병 모델동물에서 30분에서 1시간 이내로 빠르게 뇌 조직 내로 전송돼, 24 시간내에 뇌에서 대사 제거된다”라고 설명했다.
셀리버리의 퇴행성뇌질환치료제 개발실 연구책임자는 “이번 분석은 세계최고수준의 글로벌 분석기관인 코방스에서 얻은 iCP-Parkin의 혈뇌장벽 투과능력에 대한 객관적인 자료로써, 내부가 아닌 제3의 글로벌 분석기관에서 높은 수준의 뇌 전송이 증명됐다는 데에서 그 의미가 크다” 고 말했다.
추가로 “이번 결과는 현재 뇌질환치료제 개발에 가장 중요한 혈뇌장벽 투과 전략(strategy)이 뇌 내피세표의 수용체(receptor)를 통한 이중항체 전송밖에 없는 상황에서 이중항체 이외의 재조합 단백질을 뇌 혈관 내피세포 직접투과(direct penetration)라는 전혀 새로운 방법으로 뇌 조직 및 뇌신경세포에 전송할 수 있음을 입증한 결과”라고 전했다.
연구책임자는 “이는 뇌질환치료제 개발에 대한 새로운 전략인 동시에 그동안의 뇌질환치료제 개발의 난제를 극복해주는 해결책이기 때문에 글로벌 제약사들이게 할 말이 많아질 것”이라고 밝혔다.
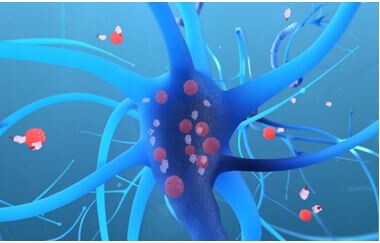 |
| ▲뇌신경세포로 투과해 들어가는 파킨슨병 치료신약 'iCP-Parkin' (사진= 셀리버리 제공) |
셀리버리가 파킨슨병 치료제 ‘iCP-Parkin’이 뇌를 지키는 보호막 혈뇌장벽을 통과해 1시간 이내로 신속하게 뇌조직에 전송된다는 것을 증명했다.
셀리버리는 글로벌 위탁연구기관 코방스 (Covance, 영국)의 액체크로마토그래피-직렬질량분석법 (LC-MS/MS)을 이용해 이 같이 입증했다고 4일 밝혔다.
최저정량한계(LLOQ)를 5000만분의 1그람 (20ng/ml) 단위까지 분석하는 정밀분석을 통해 증명한 것으로, 셀리버리는 이로써 TSDT 플랫폼기술로 향상된 약리물질의 뇌 약리동태 (Brain PK)에 대한 객관적인 데이터를 원하던 글로벌 제약사의 요구를 충족시킬 수 있게 됐다.
파킨슨병은 신경전달물질인 도파민을 생성하고 분비하는 뇌신경세포 (neuron)가 손상돼 운동능력과 인지기능에 장애가 생기는 퇴행성 뇌질환이며, 이러한 신경세포 파괴는 알파-시뉴클레인 (α-Synuclein) 단백질의 응집체 (protein aggregate)에 의해 발생한다고 알려져 있다.
파킨슨병의 치료를 위해서는 증상 완화 또는 질병의 진행을 늦추는 약물인 도파민 전구체 레보도파(Levodopa)를 투여해 뇌에서 도파민의 농도를 높여 주는 것이 유일한 약물치료법이나 장기복용 시 부장용과 약물 저항성이 나오는 등 근본적인 치료방법이라 볼 수는 없었다.
때문에 이러한 난치성 뇌질환에 대한 치료제 개발에 어려움을 극복하려 여러 글로벌 제약회사에서는 알파-시뉴클레인을 제거할 수 있는 중화 항체치료제 개발을 시도했으나 실패했다.
이는 뇌를 둘러싸고 있는 혈뇌장벽 (BBB)을 뚫고 뇌조직 안으로 약물을 전송하기가 어려움은 물론, 조금 투과하더라도 뇌신경세포 (neuron) 내부로 항체같이 커다란 약리물질들의 세포 내 투과가 불가능하기 때문이다.
그러나 셀리버리의 ‘iCP-Parkin’은 이러한 거대분자 약리물질들을 생체 내 조직, 그 조직을 구성하는 세포 안으로 약물을 전송시킬 수 있는 플랫폼기술 TSDT를 이용해 혈뇌장벽을 구성하는 혈관 내피세포 (endothelial cell) 세포막 투과에 성공했다.
이어 계속해서 뇌조직을 구성하는 뇌신경세포를 연속 투과해 알파-시뉴클레인 단백질의 응집체의 축적 (Lewy body)을 막아 파킨슨병 치료효능이 뛰어남을 상위 1% 과학저널인 사이언스 어드벤시스 (Science Advances)에 발표해 학계의 검증을 통해 증명한 바 있다.
셀리버리관계자는 “이번 결과에서 보여주는 신속한 혈뇌장벽 투과력과 뇌신경세포 안으로의 전송능력 증명은 도파민을 생성하는 신경세포에 축적되는 알파-시뉴클레인의 제거가 가능하다는 것을 시사하고 있다”고 밝혔다.
셀리버리의 퇴행성뇌질환치료제 개발실 연구책임자는 “이번 분석의 핵심은, “iCP-Parkin이 혈뇌장벽을 얼마나 신속하게 통과해 뇌조직의 심부에 들어가는지를 보여줌에 의의가 있다” 고 강조했다.
또한 “파킨슨병 모델동물에서 8 단계의 시간대별로 iCP-Parkin을 1회 꼬리정맥 주사투여한 뒤 뇌 120개와 혈액 80개의 샘플을 확보하여, 영국의 코방스로 보내 TSDT 기술이 적용된 iCP-Parkin 재조합단백질 뒤쪽 부분 (33개의 아미노산)을 감지해 조직과 혈액에서 iCP-Parkin을 정량적으로 분석했다”고 덧붙였다.
아울러 “파킨슨병 모델동물에서 30분에서 1시간 이내로 빠르게 뇌 조직 내로 전송돼, 24 시간내에 뇌에서 대사 제거된다”라고 설명했다.
셀리버리의 퇴행성뇌질환치료제 개발실 연구책임자는 “이번 분석은 세계최고수준의 글로벌 분석기관인 코방스에서 얻은 iCP-Parkin의 혈뇌장벽 투과능력에 대한 객관적인 자료로써, 내부가 아닌 제3의 글로벌 분석기관에서 높은 수준의 뇌 전송이 증명됐다는 데에서 그 의미가 크다” 고 말했다.
추가로 “이번 결과는 현재 뇌질환치료제 개발에 가장 중요한 혈뇌장벽 투과 전략(strategy)이 뇌 내피세표의 수용체(receptor)를 통한 이중항체 전송밖에 없는 상황에서 이중항체 이외의 재조합 단백질을 뇌 혈관 내피세포 직접투과(direct penetration)라는 전혀 새로운 방법으로 뇌 조직 및 뇌신경세포에 전송할 수 있음을 입증한 결과”라고 전했다.
연구책임자는 “이는 뇌질환치료제 개발에 대한 새로운 전략인 동시에 그동안의 뇌질환치료제 개발의 난제를 극복해주는 해결책이기 때문에 글로벌 제약사들이게 할 말이 많아질 것”이라고 밝혔다.
메디컬투데이 이대현 ([email protected])

[저작권자ⓒ 메디컬투데이. 무단전재-재배포 금지]