"식약처에 연내 1상 임상시험 신청할 예정"
바이오니아의 자회사 써나젠테라퓨틱스는 자사의 신장ㆍ폐ㆍ간 섬유증 등 신약후보물질(SAMiRNA-AREG)을 한 해외 제약회사가 검증시험할 수 있도록 하는 계약을 맺었다고 19일 밝혔다.
이번 계약(Feasibility Study Agreement)에 따라 써나젠으로부터 후보물질을 제공받은 계약 상대방은 전문 업체에 실험을 맡겨 치료 효과를 검증한 뒤 최종보고서를 제출해야 한다. 검증시험(Feasibility Study) 또는 물질이전(Material Transfer) 계약은 통상적으로 신약 기술이전 과정 중 하나다.
검증시험 데이터와 최종보고서 등 모든 연구결과물에 대한 소유권과 지식재산권은 써나젠이 갖는다. 써나젠은 이 후보물질에 대해 식품의약품안전처에 연내 1상 임상시험을 신청할 예정이다.
회사 관계자는 “후보물질에 대한 모델링이 단순하기 때문에 검증시험 결과 도출까지 걸리는 기간이 길지 않을 것으로 기대한다”며 “비밀유지 조항으로 인해 상세한 계약 내용을 밝힐 수 없지만 시험 결과는 후보물질이 글로벌 시장으로 나아가는 디딤돌이 될 것이라고 자신한다”고 말했다.
한편, SAMiRNA는 질병 mRNA를 분해하는 siRNA(짧은 간섭 RNA)가 인체에서 쉽게 분해되지 않고 타깃 세포까지 잘 전달돼 약효를 오래 유지하도록 양끝에 각각 친수성ㆍ소수성 물질을 결합한 단일분자 신약 플랫폼이다.
80~90㎚ 크기에 수용액에서 저절로 중성 전하를 띤 공 모양의 나노입자를 형성하기 때문에 인체 면역세포가 이물질로 인식하지 못한다. SAMiRNA-AREG는 국내에서 이뤄진 다양한 질환 모델 동물실험과 영장류 독성시험에서 만성신장질환, 원인을 알 수 없는 특발성 폐섬유증, 비알코올성 지방간염(NASH) 같은 염증ㆍ섬유증을 억제하는 효과와 안정성이 입증됐다.
내장 백색지방 조직을 70%가량 감소시키고 중성지방을 줄여주는 항비만 효과도 확인됐다. 반면, 선천면역반응 같은 부작용은 나타나지 않았다.
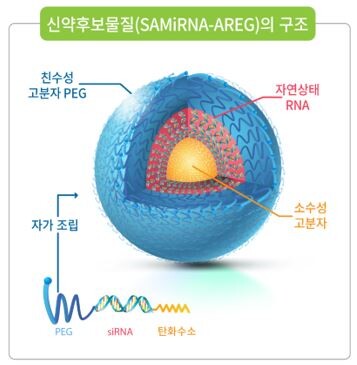 |
| ▲신약후보물질 'SAMiRNA' 구조도 (사진= 바이오니아 제공) |
바이오니아의 자회사 써나젠테라퓨틱스는 자사의 신장ㆍ폐ㆍ간 섬유증 등 신약후보물질(SAMiRNA-AREG)을 한 해외 제약회사가 검증시험할 수 있도록 하는 계약을 맺었다고 19일 밝혔다.
이번 계약(Feasibility Study Agreement)에 따라 써나젠으로부터 후보물질을 제공받은 계약 상대방은 전문 업체에 실험을 맡겨 치료 효과를 검증한 뒤 최종보고서를 제출해야 한다. 검증시험(Feasibility Study) 또는 물질이전(Material Transfer) 계약은 통상적으로 신약 기술이전 과정 중 하나다.
검증시험 데이터와 최종보고서 등 모든 연구결과물에 대한 소유권과 지식재산권은 써나젠이 갖는다. 써나젠은 이 후보물질에 대해 식품의약품안전처에 연내 1상 임상시험을 신청할 예정이다.
회사 관계자는 “후보물질에 대한 모델링이 단순하기 때문에 검증시험 결과 도출까지 걸리는 기간이 길지 않을 것으로 기대한다”며 “비밀유지 조항으로 인해 상세한 계약 내용을 밝힐 수 없지만 시험 결과는 후보물질이 글로벌 시장으로 나아가는 디딤돌이 될 것이라고 자신한다”고 말했다.
한편, SAMiRNA는 질병 mRNA를 분해하는 siRNA(짧은 간섭 RNA)가 인체에서 쉽게 분해되지 않고 타깃 세포까지 잘 전달돼 약효를 오래 유지하도록 양끝에 각각 친수성ㆍ소수성 물질을 결합한 단일분자 신약 플랫폼이다.
80~90㎚ 크기에 수용액에서 저절로 중성 전하를 띤 공 모양의 나노입자를 형성하기 때문에 인체 면역세포가 이물질로 인식하지 못한다. SAMiRNA-AREG는 국내에서 이뤄진 다양한 질환 모델 동물실험과 영장류 독성시험에서 만성신장질환, 원인을 알 수 없는 특발성 폐섬유증, 비알코올성 지방간염(NASH) 같은 염증ㆍ섬유증을 억제하는 효과와 안정성이 입증됐다.
내장 백색지방 조직을 70%가량 감소시키고 중성지방을 줄여주는 항비만 효과도 확인됐다. 반면, 선천면역반응 같은 부작용은 나타나지 않았다.
메디컬투데이 이대현 ([email protected])

[저작권자ⓒ 메디컬투데이. 무단전재-재배포 금지]
















































